已提交TGA审批!Novavax有望成澳洲第四款获批新冠疫苗(组图)
诺瓦瓦克斯公司(Novavax)已经向澳洲治疗用品管理局(TGA)提交申请,希望临时获批在澳推广诺瓦瓦克斯疫苗。

澳洲九号台新闻报道称,如果获批,那么诺瓦瓦克斯疫苗将成为继牛津-阿斯利康、辉瑞和莫德纳之后第四款在澳获批的新冠疫苗,也将成为澳洲的首款蛋白候选新冠病毒疫苗。
诺瓦瓦克斯公司还宣布,除了向TGA提出申请外,最近还向药品和医疗产品监管署(MHRA)提出了申请。
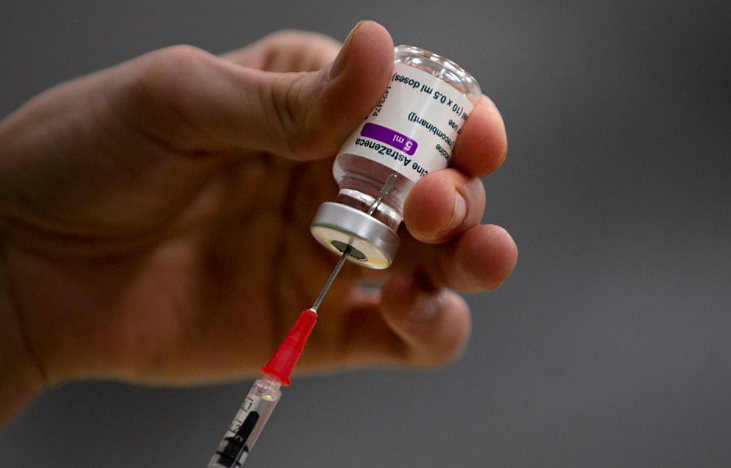
(图片来源:澳洲九号台新闻)
诺瓦瓦克斯总裁兼首席执行官Stanley C. Erck在一份声明中说,“这次提交申请使诺瓦瓦克斯公司更接近于向澳洲提供第一款蛋白新冠病毒疫苗。再加上本周向英国提出的申请,我们距离在全球广泛推广我们疫苗的目标又进了一步。我们感谢澳洲的临床试验参与者、监管部门和疫苗专家,感谢他们对这一疫苗项目的协助和贡献。”
澳洲九号台新闻指出,诺瓦瓦克斯疫苗需要接种两次,间隔时间至少21天。可储存在2℃ - 8℃的环境中,这意味着现有的冷链渠道可用于运输该型疫苗。

(图片来源:澳洲九号台新闻)
今年早些时候,诺瓦瓦克斯向TGA提交了在英国进行的有1.5万名受试者参与的临床试验数据。
根据该数据:诺瓦瓦克斯疫苗对原始病毒株的有效性达到了96.4%,对Alpha变异毒株的有效性达到了86.3%,总体有效性为89.7%。
诺瓦瓦克斯还表示,根据在美国和墨西哥进行的有3万名受试者参与的3期试验,该型疫苗预防中度和重症的有效性为100%,总体有效性为90.4%。
不过,该公司并没有公布针对目前流行的Delta变异毒株的有效性数据。
(Gleen)
专题:新冠疫情在澳大规模爆发进入专题 >>
澳洲官宣:将设立全国疾控中心!2026年1月1日起运作(组图)
澳洲发现新冠新变体,恐致夏天病例激增!专家:疫苗保护减弱(图)
新冠变异毒株“XEC”登陆澳洲!专家科普来了(图)












 +61
+61 +86
+86 +886
+886 +852
+852 +853
+853 +64
+64


